Selpercatinib zugelassen für Schilddrüsen- und Lungenkrebs mit RET-Genveränderungen
Menschen mit Schilddrüsen- oder Lungenkrebs, deren Tumoren spezifische Veränderungen in einem Gen namens RET enthalten, haben jetzt eine neue Behandlungsoption.
Am 8. Mai erteilte die Food and Drug Administration (FDA) die beschleunigte Zulassung des Arzneimittels Selpercatinib (Retevmo) zur Behandlung bestimmter Patienten mit RET- verändertem Schilddrüsenkrebs oder nicht-kleinzelligem Lungenkrebs . Das Medikament blockiert die Aktivität von RET- Proteinen .
Die Zulassung des Arzneimittels basierte auf einer Studie, in der bei mehr als der Hälfte aller Patienten mit fortgeschrittenem RET- verändertem Lungen- und Schilddrüsenkrebs, in vielen Fällen über einen Zeitraum von 6 Monaten oder länger, Tumore geschrumpft wurden. Selpercatinib, das als Pille eingenommen wird, scheint weniger Nebenwirkungen zu haben als ältere Medikamente, die die RET-Aktivität blockieren.
Die Studie zu Selpercatinib, einer klinischen Studie namens LIBRETTO-001, wurde von Eli Lilly and Company und Loxo Oncology, dem ursprünglichen Hersteller des Arzneimittels (jetzt Loxo Oncology at Lilly), gesponsert.
Selpercatinib, das erste Medikament, das selektiv gegen RET wirkt, ist "eine wichtige Entwicklung für die Behandlung von RET- veränderten Krebsarten", sagte Dr. Jaydira del Rivero, eine auf endokrine Krebserkrankungen spezialisierte Onkologin im NCI- Zentrum für Krebsforschung , die nicht daran beteiligt war die Studium.
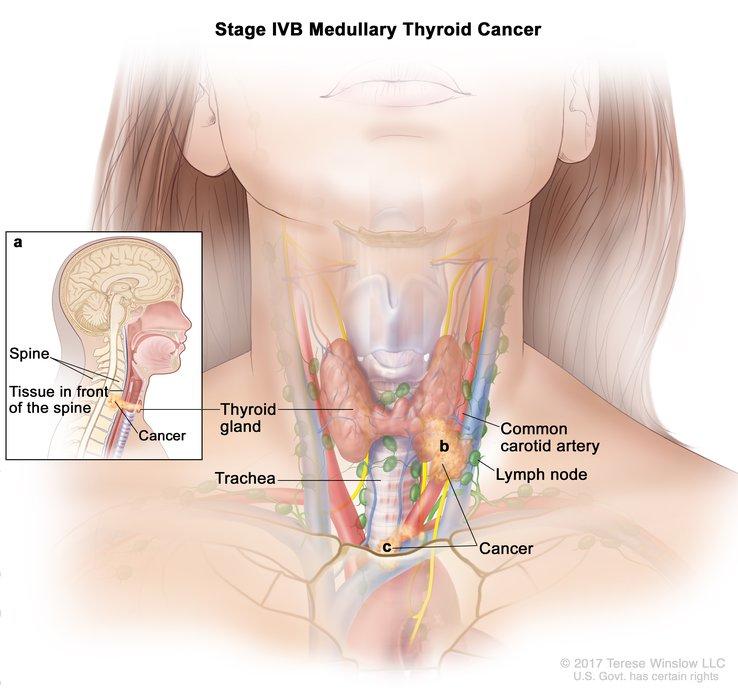
Im Rahmen der Zulassung kann Selpercatinib bei drei Gruppen von Patienten mit RET- verändertem Krebs angewendet werden: Erwachsene mit nicht-kleinzelligem Lungenkrebs, der sich ausgebreitet oder metastasiert hat; Erwachsene und Kinder ab 12 Jahren mit fortgeschrittenem oder metastasiertem medullärem Schilddrüsenkrebs, die eine systemische Therapie benötigen; und Erwachsene und Kinder ab 12 Jahren mit fortgeschrittenem oder metastasiertem papillärem Schilddrüsenkrebs , der gegen die Behandlung mit radioaktivem Jod resistent ist und eine systemische Therapie erfordert.
Eine beschleunigte FDA-Zulassung soll die Verfügbarkeit von Arzneimitteln beschleunigen, die schwerwiegende Erkrankungen behandeln und einen ungedeckten medizinischen Bedarf decken. Die Zulassung von Selpercatinib beruhte auf der Fähigkeit des Arzneimittels, Tumore zu verkleinern, und der Dauer dieser Reaktion. Weitere Studien sind von der FDA erforderlich, um zu bestätigen, dass die Behandlung den Patienten einen klinischen Nutzen bringt, beispielsweise durch eine Verbesserung ihrer Lebenserwartung.
RET- Veränderungen spornen das Krebswachstum an
RET- Veränderungen sind bei Krebs insgesamt selten, bei Lungen- und Schilddrüsenkrebs jedoch häufiger. Ungefähr 2% der Menschen mit nicht-kleinzelligem Lungenkrebs und 10% –20% der Menschen mit papillärem Schilddrüsenkrebs, der häufigsten Art von Schilddrüsenkrebs, haben Tumoren, bei denen ein Teil des RET- Gens mit einem Teil eines anderen Gens fusioniert ist , bekannt als RET- Fusions-positiver Krebs. Darüber hinaus finden sich in mehr als der Hälfte aller Fälle von medullärem Schilddrüsenkrebs kleinere genetische Veränderungen ( Mutationen ) bei RET .
Obwohl medullärer Schilddrüsenkrebs selten ist, sind die Aussichten für Menschen mit dieser Form von Schilddrüsenkrebs schlechter als für Menschen mit papillärem Schilddrüsenkrebs, sagte Lori Wirth, MD, Studienleiterin von LIBRETTO-001, vom Massachusetts General Hospital.
Fusionen und Mutationen von RET- Genen führen zur Produktion abnormaler RET-Proteine, die das Wachstum von Krebszellen ankurbeln. RET ist eine Proteinart, die als Kinase bezeichnet wird und an verschiedenen Zellprozessen beteiligt ist.
Selpercatinib “wurde entwickelt, um auf RET abzuzielen und gleichzeitig seine Aktivität gegen andere Kinasen zu minimieren. Die meisten anderen Medikamente in unserem Arsenal, die eine gewisse Aktivität gegen RET- veränderte Krebsarten aufweisen, sind Multikinasehemmer, die auf die Aktivität anderer Kinasen abzielen und diese blockieren “, sagte Dr. Wirth zusätzlich zu RET.
Obwohl diese anderen Medikamente, einschließlich Cabozantinib (Cabometyx) und Vandetanib (Caprelsa) , eine gewisse Aktivität gegen diese Krebsarten aufweisen, ist ihre Nützlichkeit bei der Behandlung von RET- veränderten Krebsarten durch ihre Nebenwirkungen begrenzt. Da diese früheren Medikamente mehrere Kinasen blockieren, ist die Wahrscheinlichkeit von Nebenwirkungen höher als bei Selpercatinib, erklärte sie.
Klinische Studienergebnisse für Patienten mit Lungen- und Schilddrüsenkrebs
Die LIBRETTO-001-Studie wurde gestartet, um Selpercatinib bei Menschen mit RET- verändertem Krebs zu testen. Alle Teilnehmer dieser Phase-1/2-Studie erhielten das Studienmedikament.
Die Ergebnisse für 105 Patienten mit RET- Fusions-positivem nicht-kleinzelligem Lungenkrebs, die zuvor mit einer Chemotherapie behandelt worden waren, wurden in einem früheren Beitrag zu Cancer Currents beschrieben . Von einer zweiten Gruppe von 39 Patienten mit RET -fusionspositivem Lungenkrebs, die zuvor nicht behandelt worden waren, sprachen 85% auf das Medikament an – das heißt, ihre Tumoren schrumpften – und 58% dieser Patienten reagierten 6 Monate oder länger.
An der Studie nahmen auch 55 Patienten mit RET- verändertem medullärem Schilddrüsenkrebs teil, die zuvor mit Cabozantinib, Vandetanib oder beiden behandelt worden waren, sowie 88 Patienten, die diese Medikamente nicht erhalten hatten. Die Ansprechraten betrugen 69% und 73% in der Gruppe vor und ohne Behandlung, und bei den meisten Patienten dauerte das Ansprechen 6 Monate oder länger.
Für die 19 Patienten in der Studie mit RET -fusionspositivem Schilddrüsenkrebs, deren Krankheit nicht mehr auf die Behandlung mit radioaktivem Jod ansprach und zuvor eine systemische Behandlung erhalten hatte, und 8 Patienten, die nur radioaktives Jod erhalten hatten, lagen die Ansprechraten bei 79% und 100%. beziehungsweise. Diese Reaktionen dauerten bei vielen Patienten 6 Monate oder länger.
"Wir haben nicht nur hohe Rücklaufquoten gesehen, sondern die Rückläufe waren auch sehr langlebig", sagte Dr. Wirth. Die Ermittler verfolgen weiterhin die Patienten in der Studie, und die meisten Patienten, die ursprünglich auf das Medikament angesprochen hatten, sprechen immer noch an, sagte sie.
Die häufigsten Nebenwirkungen von Selpercatinib waren Durchfall, Bluthochdruck und erhöhte Blutspiegel von zwei Leberenzymen – ein Zeichen für Lebertoxizität. Schwerwiegende Nebenwirkungen, einschließlich abnormaler Herzrhythmen und Lungenentzündung, traten bei einem Drittel aller Patienten in der Studie auf.
Während die meisten Nebenwirkungen behandelt werden konnten, brachen 5% der Patienten die Behandlung wegen schwerwiegender Nebenwirkungen dauerhaft ab.
Eine vielversprechende Option für Krebserkrankungen mit RET- Änderungen
"Es ist nicht nur so, dass wir ein neues Medikament zur Behandlung unserer Patienten mit RET- verändertem Schilddrüsenkrebs haben, sondern das Medikament hat auch eine wirklich gute Aktivität und ein gutes Nebenwirkungsprofil" im Vergleich zu anderen von der FDA zugelassenen Behandlungen für Schilddrüsenkrebs, Dr. Sagte Wirth.
Dr. del Rivero sagte auch, dass Selpercatinib Schilddrüsentumoren mit einer RET V804-Mutation schrumpfte, die gegen andere Therapien resistent sind.
Es ist immer noch nicht bekannt, ob Selpercatinib den Patienten hilft, länger zu leben, fuhr sie fort. Sie sagte jedoch, dass die bisherigen Ergebnisse darauf hindeuten, dass das Medikament letztendlich die Erstbehandlung für Menschen mit RET- verändertem Krebs, insbesondere medullärem Schilddrüsenkrebs, sein wird.
"Weitere Informationen sind erforderlich, aber wir sind optimistisch in Bezug auf diese Behandlung", fügte Dr. del Rivero hinzu.
Um diese zusätzlichen Informationen bereitzustellen, hat Eli Lilly eine klinische Phase-3-Studie gestartet, in der Selpercatinib bei Patienten mit fortgeschrittenem, RET- mutiertem medullärem Schilddrüsenkrebs entweder mit Cabozantinib oder Vandetanib verglichen wird. Dr. Wirth sagte jedoch, die COVID-19-Pandemie habe die Aufnahme von Patienten in die Studie an einigen Studienorten, einschließlich ihres Krankenhauses, vorübergehend verlangsamt oder gestoppt.
Schließlich sagte Dr. Wirth: „Jetzt, da wir eine wirklich gute RET-spezifische Therapie haben, müssen wir sicherstellen, dass Ärzte und Patienten wissen, dass es wichtig ist, Genomtests an Tumorproben von Patienten mit medullärem Schilddrüsenkrebs durchzuführen, um diese zu finden heraus, wenn sie Änderungen in RET enthalten .
Quelle: National Cancer Institute